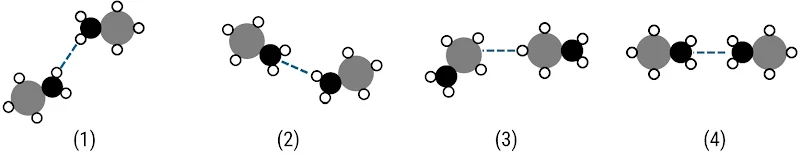
Câu 10. Mô hình VSEPR (Valence Shell Electron Pair Repulsion) được sử dụng để mô tả dạng hình học của các phân tử dựa trên lực đầy giữa các...
Đề bài
Câu 10. Mô hình VSEPR (Valence Shell Electron Pair Repulsion) được sử dụng để mô tả dạng hình học của
các phân tử dựa trên lực đầy giữa các cặp electron hoá trị.
“Các cặp electron hoá trị được phân bố xung quanh nguyên tử trung tâm sao cho lực đẩy giữa chúng là nhỏ nhất".
Để sử dụng mô hình VSEPR, công thức phân tử của chất được viết dưới dạng AXnEm.
Trong đó:
A: nguyên tử trung tâm;
X: nguyên tử liên kết với nguyên tử A; n là số nguyên tử X;
E: cặp electron hoá trị chưa liên kết của nguyên tử A; m là số cặp electron E;
Nếu nguyên tử trung tâm lẽ một electron thì electron đó vẫn được tính tương đương một cặp electron.
Dạng mô hình VSEPR và cấu trúc phân tử có đặc điểm như sau
Phát biểu nào sau đây không đúng ?
A. Phân tử CH4 viết theo mô hình VSEPR là AX4.
B. Công thức của H2O theo mô hình VSEPR là AX2E2.
C. Dựa vào mô hình VSEPR dự đoán dạng hình học của phân tử NH3 có dạng tam giác phẳng.
D. Dựa vào mô hình VSEPR dự đoán phân tử H2O có dạng góc.