Câu 3. Cho các bước thực hiện thí nghiệm: Phản ứng thế bromine vào hexane
Dụng cụ: Ống nghiệm, ống hút nhỏ giọt, kẹp gỗ, giá để ống nghiệm.
Hóa chất: Hexane, nước bromine.
Tiến hành:
Bước 1: Lấy 2 ống nghiệm, dùng ống hút nhỏ giọt cho vào mỗi ống nghiệm khoảng 2 mL nước bromine.
Bước 2: Dùng ống hút nhỏ giọt nhỏ tiếp khoảng 2 mL hexane vào cả hai ống nghiệm, lắc đều. Sau đó đưa ống nghiệm (1) ra nơi có ánh sáng mặt trời (hoặc ngâm trong cốc nước nóng khoảng 50 0C). Ống (2) để nguyên trong phòng tối. Quan sát hiện tượng xảy ra ở hai ống nghiệm.
Cho các phát biểu sau:
A. Sau bước 1: các ống nghiệm có hai lớp, lớp dưới là bromine màu vàng, lớp trên là hexane không màu.
B. Ống 1 xảy ra phương trình hoá học: Br2 + C6H14 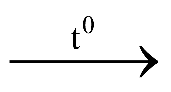 C6H13Br + HBr.
C6H13Br + HBr.
C. Phản ứng trên chứng tỏ alkane dễ dàng phản ứng nước bromine ngay ở điều kiện thường.
D. Cho biết độ tan của Br2 trong nước là 3,5 gam/L và trong hexane là 250 gam/L. Cho 10 mL nước bromine có d = 3,1 gam/mL vào phễu chiết và tiến hành chiết bromine bằng hexane. Để chiết được 90% lượng Br2 trong nước thì thể tích hexane cần dùng là 12,6 mL.